摘要
恶液质(cachexia)是一个全球范围的严重疾病,发病率逐年递增,常伴发于多种慢性疾病。其中,肿瘤恶液质(cancer cachexia)发病率最高,是各种晚期恶性肿瘤的常见并发症,进展期恶性肿瘤约60%~80%可出现恶液质,约20%肿瘤患者死于恶液质。因此,肿瘤恶液质的准确临床诊断和制定有效干预措施对于晚期恶性肿瘤患者的长期生存具有重要意义。基于此,中国抗癌协会肿瘤营养专业委员会依据肿瘤恶液质筛查、诊断、评估、治疗等方面研究证据和临床经验进行分析、讨论和总结,制订了《肿瘤恶液质临床诊断与治疗指南(2020版)》,以供临床医师参考。
概述
恶液质(cachexia)是一种与慢性病相关的营养不良性疾病, 往往伴随非特异性炎症, 是营养不良的特殊形式[1]。目前较为公认的恶液质定义是: 以持续性骨骼肌消耗为特征, 伴或不伴有脂肪组织丢失, 常规营养治疗不能完全缓解, 最终可导致进展性功能损伤的多因素综合征[2]。恶液质常伴发于多种慢性疾病, 包括恶性肿瘤、慢性阻塞性肺病、慢性心衰、慢性肾衰、肝功能不全、艾滋病和风湿性关节炎等。其中, 肿瘤恶液质(cancer cachexia)发病率高, 是各种晚期恶性肿瘤(后文简称肿瘤)一种常见的并发症, 其以骨骼、内脏的肌肉消耗为特征, 伴有食欲减退、厌食、饱胀感、体质量下降、肌肉萎缩、乏力、贫血、水肿、低蛋白血症等多种临床表现。有报道显示, 60%~80%的肿瘤患者可能出现恶液质, 约20%的肿瘤患者死于肿瘤恶液质[3]。因此, 肿瘤恶液质的准确临床诊断和有效干预措施对于晚期癌症患者的长期生存具有深远意义。
1.恶液质制定基本信息
1.1 目标
本指南的总体目标是将已有证据和专家意见转化为多学科团队的诊疗建议, 针对肿瘤患者的代谢紊乱, 实现早发现和早治疗; 为医护人员提供指导, 以最适当和有效的干预手段处理肿瘤患者的营养和代谢问题; 降低肿瘤患者恶液质的发生率、严重程度和不良影响。
1.2 方法
1.2.1 研究策略 本指南中各部分内容由中国抗癌协会肿瘤营养专业委员会委员及其团队负责, 通过评估现有证据, 制定推荐内容, 并评估应用指南获得的临床效益、成本和风险。在推荐级别制定过程中, 对于有高级别证据的内容, 推荐强度则依赖于证据强度; 而对于恶液质诊疗的大多数临床问题, 已有的研究尚未发现能逐一解决, 证据或仅有低、中级别证据, 认为其属于证据不足情况, 指南制定小组则使用专家共识达成一致意见后提出推荐强度, 并在其后用"共识性建议"明确标出。专家共识实施步骤依照Delphi调查法, 专家以证据级别为基础, 根据其临床可行性和可获得性等多方面考虑后进行相应推荐, 是包含专家主观意见的共识性建议。具体推荐类型和推荐级别、证据水平在本指南中与推荐意见一同提供。
1.2.2 制定流程 本指南是一个基于系统性回顾与专家共识,并由多学科专家小组制定的指南。本文通过对中国知网、中国生物医学文献数据库、万方中国学术期刊数据库等国内核心数据库,以及PubMed、Embase、Google Scholar和Cochrane数据库等国际核心数据库进行了基于“癌症”“、恶液质”“、治疗”“、诊断”“、Cancer”、“Cachexia”“、Treatment”“、Diagnosis”等核心检索词/主题词的系统性文献检索。符合以下条件的文章被排除在系统性回顾之外:未在同行评审期刊上发表的会议摘要;社论、评论、信件、新闻文章、案例报告、叙述性评论。
专家共识Delphi调查法:1)向专家小组提出问题和有关要求,并附上相关背景材料,各位专家基于相关材料提出自己的推荐意见,并说明相应依据;2)将各位专家的第一次判断意见汇总、列出、对比,再分发给各位专家,由专家将自己的意见与其他专家的意见进行比较,修改自己的意见和判断;3)收集所有专家的修改意见,汇总,再分给各位专家进行二次修改;4)收集意见和信息反馈一般需要经过三、四轮,直至每位专家均同意为止;5)对专家的意见进行综合处理,确认最终确定指南推荐建议。
2.恶液质的发病机制
与单纯的营养不良不同, 恶液质也与代谢异常有关[4-8]。肿瘤相关基因的过度表达导致引起分解代谢的介质增加, 同时癌症引发的炎症可以产生促炎细胞因子。肿瘤恶液质患者代谢异常的主要特点: 能量消耗增加、蛋白质和(或)脂肪分解增加和蛋白质合成减少等, 其主要机制可能涉及包括神经-内分泌激素失调、炎症及炎症因子[肿瘤坏死因子-α(tumor necrosis factor-α, TNF-α)、白介素(interleukins, ILs)]、特殊代谢因子(脂肪动员因子)和蛋白水解诱导因子等。
3.肿瘤恶液质筛查与诊断
3.1 筛查
早期恶液质筛查对于癌症患者营养状态的逆转和生存期的改善至关重要。本指南参考欧洲进展期肿瘤患者实用临床恶液质指南,推荐的筛查方法及其内容见表 1。
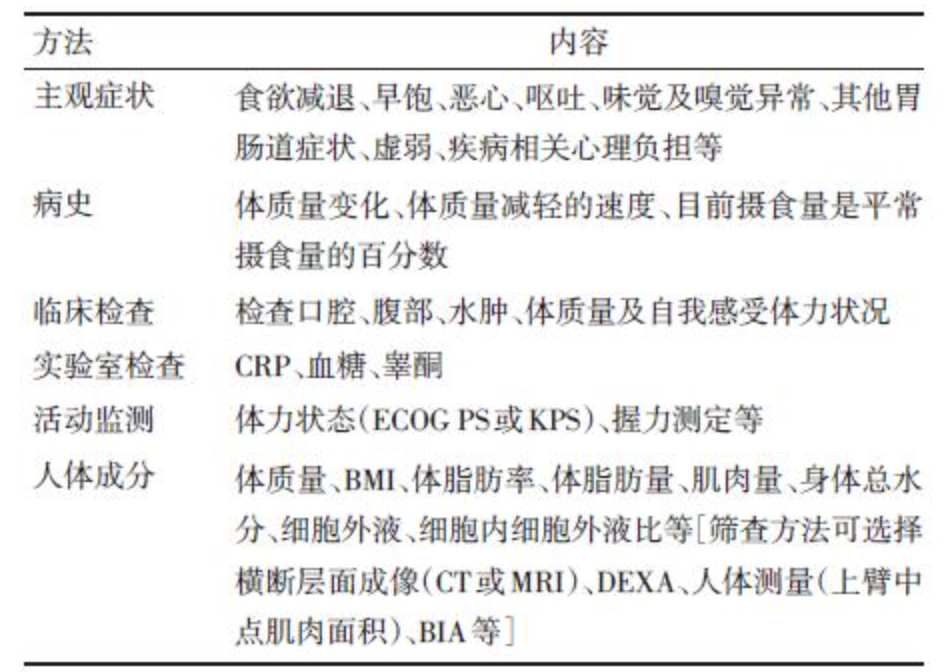
表 1 恶液质筛查
一项前瞻性研究[9]显示, 基于肿瘤类型(低危: 乳腺癌、淋巴瘤、白血病; 高危: 胰腺癌和胃癌; 中危: 其他癌症)、食欲减退和慢性阻塞性肺疾病等信息, 可提高对恶液质预测的准确性。在体质量未下降或体质量下降很少(< 3%)的患者中尤其重要。基于这些预测信息, 患者可以分为五个不同的恶液质发展风险水平(风险级别1:体质量下降 < 3%, 低危肿瘤类型, 并且无/少食欲下降; 风险级别2: < 3%体质量下降, 低危肿瘤类型和相当/严重食欲下降, 或中危肿瘤类型和无/少食欲下降; 风险级别3: < 3%体质量下降, 中风险肿瘤类型,以及相当/严重食欲下降;风险级别4:高危肿瘤类型;风险级别5:体质量下降3%~5%)。如果处于风险级别1,则不太可能发生恶液质,而对于风险级别为3或以上的患者,发生恶液质的风险很高。因此,临床医生可参考风险级别密切地跟踪患者恶液质的发展,及时诊断并早期进行充分的治疗干预,但此风险分级的有效性仍有待在今后的临床实践中验证。
3.2 诊断标准
肿瘤恶液质诊断标准[2, 6]:1)无节食条件下,6个月内体质量减轻 > 5%;2)身体质量指数(body mass index,BMI) < 20 kg/m2(欧美人)、BMI < 18.5 kg/m2(中国人)和6个月内任何程度的体质量减轻 > 2%;3)四肢骨骼肌指数符合肌肉减少症标准(男性 < 7.26 kg/m2,女性 < 5.45kg/m2)和任何程度的体质量减轻 > 2%(采用欧洲姑息治疗研究协会标准);4)均需摄食减少/系统性炎症。
郭澄教授团队采用血清和尿液代谢组学分析差异代谢物,构建了一个肿瘤恶液质即时诊断数学方程:Log(P)=-400.53-481.88×log(肌肽)-239.02×log(亮氨酸)+383.92×log(乙酸苯酯)。可根据此方程评估值划分恶液质、恶液质前期和无恶液质患者,曲线下面积高达0.991,约登指数为0.895,准确率达94.64%[10]。但此检测目前难以普及,可酌情参考应用,其可行性有待进一步临床验证。
3.3 分类和分期标准
根据病因,肿瘤恶液质可以分为两类:1)原发性恶液质:直接由恶性肿瘤本身引起;2)继发性恶液质:由营养不良或基础疾病导致。恶液质是可被早期发现,并可进行有效干预的,而当其发展至晚期,抗肿瘤治疗及营养治疗均很难见效。因此,对恶液质进行分期很重要。按照病程,将肿瘤恶液质分为3期:恶液质前期、恶液质期、恶液质难治期。
目前比较公认的分期标准为:1)恶液质前期:表现为厌食和代谢改变,6个月内无意识体质量减轻≤5%;2)恶液质期:6个月内无意识体质量减轻 > 5%(排除单纯饥饿);或BMI < 20 kg/m2(中国人为BMI < 18.5 kg/m2),6个月内体质量减轻 > 2%;或四肢骨骼肌指数符合肌肉减少症诊断标准(男性 < 7.26 kg/m2;女性 < 5.45 kg/m2),同时体质量减轻 > 2%;常有摄食减少或系统性炎症;3)难治期/顽固性恶液质期:肿瘤持续进展,对治疗无反应;分解代谢活跃,体质量持续减轻无法纠正。必须指出,在此分期中,对难治性恶液质的诊断标准尚无共识。
于世英教授团队提出了一个快速诊断恶液质的分期评分表(cachexia staging score, CSS)[11](表 2)。累计得分: 0~2分, 无恶液质; 3~4分, 恶液质前期; 5~8分, 恶液质期; 9~12分, 恶液质难治期。与传统方法相比, CSS临床区分能力更强, 预后预测更准, 操作更为简便。但其准确性仍需在临床中不断实践[证据等级: 低; 推荐级别: 中度推荐(共识性建议)]。
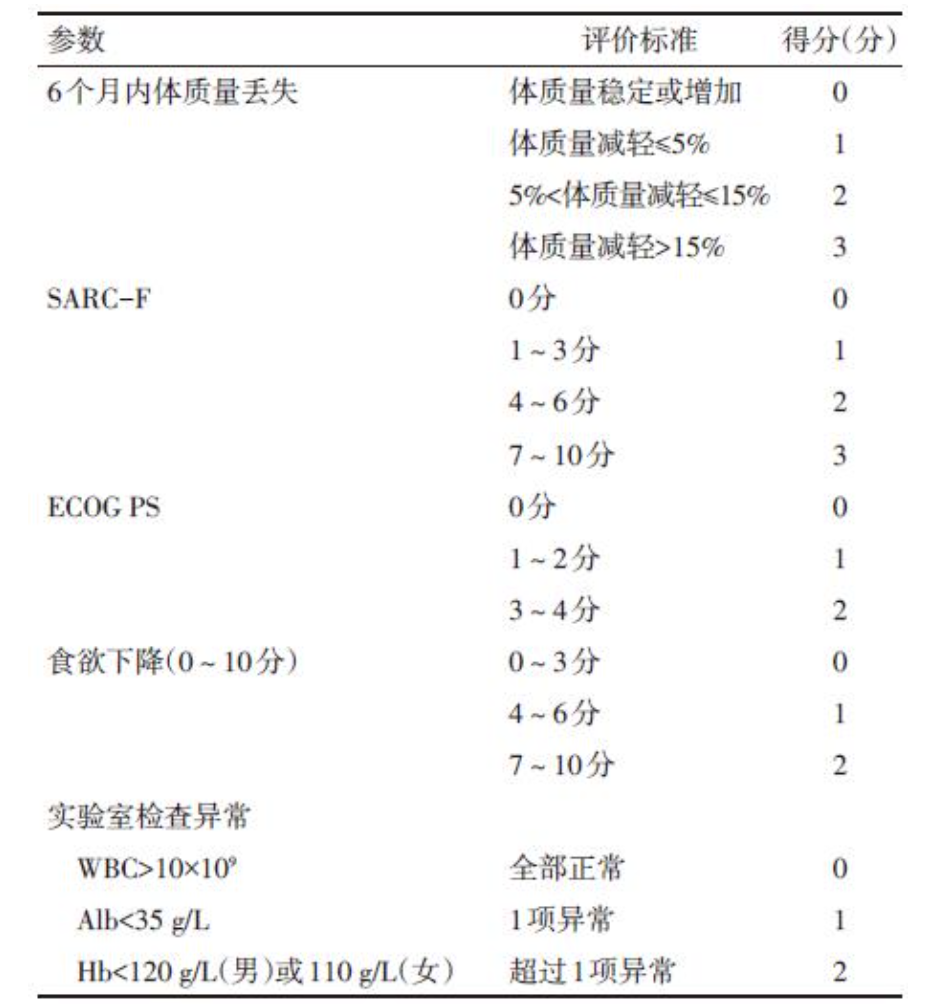
表 2 恶液质分期评分表
此外,其他恶液质分期工具在不断探索中。恶液质评分(cachexia score,CASCO)已被提出可作为肿瘤恶液质患者分期的可能有效工具,其评分内容包括5个部分:1)体质量减轻和组成成分;2)炎症/代谢紊乱/免疫抑制;3)体能状态;4)厌食;以及5)生存质量。Argilés等[12]为显示CASCO的度量特性,根据统计学方法得到的结果建立了3组不同程度恶液质:轻度恶液质(15≤X≤28)、中度恶液质(29≤X≤46)和重度恶液质(47≤X≤100)。此外,研究还提出了CASCO的简化版本MiniCASCO,有助于更简易、有效地进行恶液质分期。CASCO和MCASCO为肿瘤恶液质患者的定量分期提供了一种新的工具,与以往的分类相比具有明显优势。尽管目前尚无足够的研究证据证明CASCO的敏感性和特异性,但其在恶性肿瘤患者的有效性评估中得分较高,能够定量地对恶液质进行分期[13]。今后仍需更多的研究来验证其在恶液质人群或普通人群中的有效性[证据等级:低;推荐级别:中度推荐(共识性建议)]。
4.肿瘤恶液质评估
在诊断恶液质后,进行营养干预前,还需进一步评估以下3个方面:体质量减轻(包括肌肉质量及肌力)、摄入量(包括厌食情况)及炎症状态,而后才可针对性地进行治疗。
本文推荐患者主观整体评估(patient-generated subjective global assessment,PG-SGA)作为恶液质患者的营养评估工具量表,推荐厌食恶液质问卷(the functional assessment of anorexia-cachexia therapy,FAACT)作为厌食症/恶液质治疗的功能性评估[14]。此外,人体成分分析已成为确定患者是否有恶液质风险的重要指标。同时,评估过程中需动态监测,以评估肿瘤对机体的影响,以及肿瘤治疗对身体成分的影响[证据等级:低;推荐级别:强烈推荐(共识性建议)]。
作为恶液质的特征之一,肿瘤患者的肌肉减少应动态监测。在评估肌肉减少时,横断面成像技术,双能X线吸收法扫描和其他手段可考虑用于肿瘤恶液质患者。CT成像是一种较为理想的恶液质评估工具,较多应用于临床研究,但考虑其费用及实施程度,目前作为临床实践标准手段的应用尚为局限。
目前对营养评估的研究尚不足,缺乏前瞻性研究验证,尚未发现能逐一解决这些证据或仅有低级别证据的因素,主要依据专家小组结合现有证据和临床经验进行研讨后的结果。目前,专家普遍认为适时、动态应用目前公认的营养评估法进行评估,有助于医生确定患者是否有恶液质风险,以此制定有效治疗策略。基于此,本指南认为应重视营养评估,其对肿瘤恶液质患者具有重要意义。
5.肿瘤恶液质治疗
5.1 营养干预
从临床结局来看,营养干预可提高恶液质患者生存质量,甚至延长患者生存期。在难治性恶液质期,营养干预可能无法完全逆转其体质量减轻及代谢异常,还要考虑营养干预带来的风险和负担可能超过其潜在益处,但适当的营养摄入仍可能改善患者生存质量,并给患者及家属带来心理安慰。另外,对难治性恶液质的识别有助于患者得到临终关怀团队的帮助。恶液质营养干预的最终目标是逆转患者体质量减轻和肌肉丢失, 而对难治性恶液质患者则主要是减轻恶液质相关症状、提高整体生存质量。
5.1.1 营养咨询和饮食指导 由专业营养师(配合临床医师)进行的密切随访(包括关注营养状况、营养咨询和饮食指导)可能提高患者生存质量, 甚至延长患者生存期。经过营养咨询和饮食指导从而增加能量和蛋白质的摄入已被证明是有效的, 能改善肿瘤患者的营养状况。由专业营养师为晚期肿瘤、食欲减退和(或)体质量下降的晚期肿瘤患者进行评估和咨询, 目的是为患者及家属提供实用和安全的营养建议; 提供关于摄入高蛋白、高热量、高营养型食物的指导; 以及修正任何未经证实的或极端的饮食建议[证据等级: 低; 推荐级别: 强烈推荐(共识性建议)]。
5.1.2 肠内营养 肠内营养是经胃肠道提供代谢需要的营养物质及其他各种营养素的营养支持方式, 途径包括口服及管饲, 后者主要有鼻胃管、鼻肠管、经皮内镜下胃造瘘置管和经皮内镜下胃空肠造瘘置管等。以下3种情况建议给予肠内营养从而提高或维持营养状况: 摄入不足导致的体质量减轻; 预计7天不能进食; 超过10天进食量不足每日推荐量60%。另外, 对于无法治愈的患者, 在患者同意的前提下, 建议给予肠内营养以减轻症状, 提高生存质量, 甚至可以延长患者生存期。但是当存在系统性炎症时, 单纯通过肠内营养恢复体质量比较困难。对于进展期恶性肿瘤患者, 单纯营养干预不能带来生存获益, 但当针对代谢异常治疗时, 可能会有积极的结果。
总体推荐: 肠内营养对部分患者是有效的。对于难治性恶液质阶段的患者, 在不增加进食相关不适的情况下, 可给予肠内营养[证据等级: 低; 推荐级别: 不做常规推荐, 需根据适应证进行选择(共识性建议)]。
5.1.3 肠外营养 有营养不良的肿瘤患者, 在进行抗肿瘤治疗的同时, 若无法实施肠内营养, 建议给予全肠外营养或补充性肠外营养。短期肠外营养可针对性地提供给部分患者, 如患有可逆性肠梗阻、短肠综合征或其他导致吸收不良的疾病。在避免再喂养综合征的情况下, 补充性肠外营养可能使患者获益。
总体推荐: 针对进展期恶性肿瘤患者, 营养治疗应以肠内营养优先, 肠外营养为辅, 内外结合, 内外转换。大部分情况下不推荐单独使用肠外营养, 特别是对于难治性恶液质, 需考量肠外营养带来的不良反应[证据等级: 低; 推荐级别: 不做常规推荐, 需根据适应证进行选择(共识性建议)]。
5.1.4 营养素的应用 ω-3脂肪酸: 炎症反应促进恶液质的发生发展, 尤其在体质量减轻的恶性肿瘤患者中, 炎症进程非常强烈, 炎症状态所介导的高分解代谢大量消耗了患者摄入的营养物质。具有抗炎效应的ω-3多不饱和脂肪酸, 包括二十碳五烯酸和二十二碳六烯酸, 在恶液质中的作用受到关注。一项研究评估了口服营养干预是否对接受放化疗的恶性肿瘤患者的一系列营养和临床结果产生影响, 结果表明, 营养干预对体质量有正性影响, 其中ω-3脂肪酸的补充使患者体质量增加约2千克[15]。未来需更多的临床试验进一步验证其作用[证据等级: 低; 推荐级别: 弱推荐(共识性建议)]。
支链氨基酸: 补充支链氨基酸(branched chain amino acid, BCAA)改善肿瘤恶液质患者的营养状况尚缺乏足够的临床研究证据。BCAA可抑制蛋白分解, 同时促进蛋白合成, 具有改善食欲减低的效果。Hunter等[16]对9例腹腔内转移性腺癌患者先后给予普通全肠外营养(含BCAA 19%)或富含BCAA的全肠外营养(BCAA 50%), 结果显示富含BCAA组患者酪氨酸氧化下降(提示蛋白质利用改善)、蛋白质及白蛋白合成增加, 表明BCAA对肿瘤恶液质有明显的正效应[证据等级: 低; 推荐级别: 弱推荐(共识性建议)]。
维生素、矿物质和其他膳食补充剂: 维生素和矿物质的供应量应大致等于膳食营养参考摄入量中的推荐摄入量, 在无特殊需要的情况下不鼓励使用高剂量的微量营养素[证据等级: 低; 推荐级别: 中度推荐(共识性建议)]。
5.2 药物干预
目前美国食品和药物管理局尚未批准任何药物用于肿瘤恶液质的治疗[17]。
孕激素类似物: 孕激素类药物能增加患者食欲及进食量、增加体质量, 改善营养指标。醋酸甲地孕酮(megestrol acetate, MA)是一种人工合成的、具有口服活性的孕激素衍生物。与服用安慰剂相比, 肿瘤患者服用MA更可能改善食欲和生存质量。然而, 与使用MA相关的体质量增加主要是脂肪组织而不是骨骼肌的增加, 并且MA会增加血栓栓塞、水肿和肾上腺功能抑制的风险[18]。此外, 有研究显示MA与其他药物(沙利度胺、L-左旋肉碱以及二十碳五烯酸)联合治疗肿瘤恶液质可能有更好的作用, 或许是一种更有效的治疗方法[19-20][证据等级: 中; 推荐级别: 中度推荐(共识性建议)]。
奥氮平和醋酸甲地孕酮的联合用药: 有研究发现, 与单药MA相比, 接受奥氮平和MA的晚期胃肠道肿瘤或肺癌患者的体质量增加, 食欲和生存质量均有所改善[21]。然而, 在推荐奥氮平或米氮平作为肿瘤恶液质的常规治疗药物之前, 仍需更多临床证据[证据等级: 中; 推荐级别: 暂不推荐(共识性建议)]。
阿莫瑞林:生长激素释放肽(ghrelin)是含有28个氨基酸的肽激素,主要由胃底的泌酸腺分泌。Ghrelin可与其受体GHS-R1a结合,促进垂体释放生长激素,从而增加健康人的食欲和卡路里的摄入量。阿莫瑞林(anamorelin)是一种选择性GHS-R1a激动剂,已成为肿瘤恶液质靶向治疗的研究热点,也是迄今为止评估最严格的恶液质治疗药物。ROMA-NA3是针对两个Ⅲ期双盲研究的安全性扩展研究,该试验评估了阿莫瑞林在晚期NSCLC恶液质患者中的安全性和有效性,结果显示,阿莫瑞林可增加患者体质量并缓解厌食等症状[22]。现有证据表明,阿莫瑞林能够增加体质量,但不能改善握力[22-24]证据等级:中;推荐级别:暂不推荐(共识性建议)]。
糖皮质激素:糖皮质激素也能改善食欲,其程度与MA相似。既往发表的一篇综述指出,若干研究发现应用皮质类固醇后可改善食欲,但并不总能达到统计学上的显著性,同时缺乏足够的证据来推荐最有效的皮质类固醇药物、剂量和治疗持续时间[25]。此外,一项多中心研究表明,可通过姑息性表现量表、嗜睡和厌食基线程度来预测糖皮质激素治疗晚期肿瘤患者厌食症的疗效[26]。然而,长期使用糖皮质激素的任何营养优势均会因其不良反应(如肌肉萎缩和免疫抑制)的风险而被否定,晚期患者可以被列为潜在的糖皮质激素干预对象,因为其对于终末期肿瘤的积极药理学效应可能超过不良反应的风险。因此,作为食欲刺激剂应用时,糖皮质激素通常仅限于预期寿命为几周至几个月的患者[证据等级:中;推荐级别:弱推荐(共识性建议)]。
大麻类:医用大麻治疗肿瘤恶液质的作用尚不清楚。一项纳入289例患者的Ⅲ期多中心随机双盲对照临床试验表明,与安慰剂相比,口服大麻提取物和δ-9-四氢大麻酚在改善晚期肿瘤患者的食欲和生存质量方面并无显著差异[27]。近年一项小样本研究显示,每天服用大麻胶囊的患者,能在一定程度上改善食欲和情绪,减轻疼痛和疲劳感,但亦未达到显著性差异,尽管其中有17.6%(3/17)的患者体质量增加≥10%[28]。基于目前的文献,大麻素用于治疗肿瘤相关恶液质厌食综合征的证据仍不确切[29]。目前尚缺乏使用大麻对恶性肿瘤患者食欲或恶液质影响的可靠证据,因此不建议常规使用医用大麻作为食欲刺激剂[证据等级:低;推荐级别:暂不推荐(共识性建议)]。
雄激素或选择性雄激素受体调节剂:一项双盲、安慰剂对照的随机临床试验[30]在28例患者中评估了每周注射1次睾丸酮庚酸酯对恶液质的作用,结果显示安慰剂组的体质量减轻和瘦体质量降低更明显,而雄激素组的身体机能得到改善。但目前尚无一致的临床证据推荐使用雄激素及选择性雄激素受体调节剂来增加肌肉质量[证据等级:低;推荐级别:暂不推荐(共识性建议)]。
非甾体抗炎药:许多非甾体抗炎药已经单独或与其他药物联合用于与肿瘤恶液质相关的各种疾病状况研究。然而,目前的研究证据不足以推荐非甾体抗炎药用于治疗临床试验外的肿瘤恶液质[31][证据等级:低;推荐级别:暂不推荐(共识性建议)]。
沙利度胺:沙利度胺可以抑制TNF-α和IL-6的产生。但目前尚无足够的证据支持或反对使用沙利度胺治疗肿瘤恶液质[24, 32][证据等级:低;推荐级别:暂不推荐(共识性建议)]。
L-左旋肉碱:L-左旋肉碱不仅能增加肌肉质量,还可改善体能。在一项随机Ⅲ期临床试验中[33],L-左旋肉碱治疗有效地提高了肿瘤恶液质患者格拉斯哥预后评分以及ECOG评分。Cruciani等[34]在27例L-左旋肉碱缺乏的进展期恶性肿瘤患者中发现,添加L-左旋肉碱可改善恶性肿瘤患者的疲倦感、睡眠和抑郁症状。但是,仍缺乏高质量的证据来确定补充左旋肉碱可作为恶液质的治疗策略[证据等级:低;推荐级别:暂不推荐(共识性建议)]。
中医药辅助治疗:现阶段,国内中医对肿瘤恶液质的临床研究主要围绕在营养补充或联合孕激素的基础上应用与不应用中药开展。何林巧等[35]在一项小规模随机对照研究中发现扶正口服液可增加肿瘤恶液质患者的体质量、进食量,提高KPS评分,且可提高血红蛋白及血清白蛋白量;苏雅等[36]发现以中药八珍汤为基础辨证治疗肿瘤恶液质有助于增加体质量,改善患者生存质量,从而延长生存期;而宋娜等[37]研究发现在改善患者中医证候积分方面,无论在短期疗效还是长期疗效中,调胃醒脾方在改善患者中医症状积分方面,对纳差、腹胀症状的改善均优于醋酸甲地孕酮。目前,中医药辅助治疗恶液质的报道逐渐增加,但大多规模较小,且方剂剂型不尽相同,未来仍需深入研究中医药在恶液质治疗中的作用。基于现有研究结果与临床实践经验,不可否认,中医药辅助治疗对肿瘤恶液质具有一定的积极作用[证据等级:中;推荐级别:中度推荐(共识性建议)]。
5.3 其他干预
5.3.1 体力锻炼 一项关于运动与恶液质的横断面临床研究表明,爬楼梯力和上半身肌力可作为肿瘤恶液质患者功能损害的鉴别指标[38]。运动通过调节细胞因子的表达,并可能与激素合成协同作用,从而改善力量、肌肉功能和生存质量[39]。运动可增加胰岛素敏感性,提高蛋白合成效率,降低炎症反应,提高免疫反应。在小规模试验中,抗阻运动与睾酮联合应用对老年恶液质的合成代谢作用比单独干预更大[40]。因此,运动联合营养干预或其他干预的模式可能成为治疗恶液质的有效手段,有望成为多学科治疗的重要组成部分[41]证据等级:高;推荐级别:强烈推荐(共识性建议)]。
5.3.2 心理社会干预 肿瘤恶液质患者常存在负性心理社会效应[42]。一项针对晚期肿瘤患者体质量和饮食相关痛苦的心理社会干预的分组随机试验表明,采用麦克米伦方法进行心理社会干预,可减缓晚期肿瘤患者的体质量减轻、厌食等恶液质综合征症状[43]。另有研究提示,无论是头颈癌、肺癌、胃肠道癌、乳腺癌、睾丸癌或卵巢癌患者,治疗期间应用心理教育,可增强饮食相关的自我管理能力,从而降低恶性肿瘤放化疗期间的营养风险[44-45]。心理社会支持作为多学科治疗的一部分[46],有可能缓解患者痛苦和家庭冲突,为患者提供心理支持,减少社会孤立并鼓励患者坚持治疗[证据等级:低;推荐级别:中度推荐(共识性建议)]。
6.结语
针对恶液质前期或恶液质期的高危人群,早期识别、积极预防和及时干预是逆转恶液质潜在的严重不良后果的重要手段;而对于难治性恶液质期患者,即使进行积极有效的治疗,其体质量丢失及代谢异常可能无法完全逆转,应尽力稳定恶液质,减轻其相关症状,防止或延缓恶液质进一步发展,提高整体生存质量。随着对恶性肿瘤、恶液质、生物标记物和人体成分变化的了解不断加深,治疗肿瘤恶液质的最佳方法可能涉及单一或联合策略,包括药物干预、营养干预、运动指导和心理干预。在循证医学基础上,多学科诊疗小组领导下的综合治疗是肿瘤恶液质的最佳治疗模式。

|



